肠道“小厨师”大显身手!Science:揭示一种肠道微生物酶具有惊人的代谢能力,助力营养不良儿童健康成长
来源:生物谷原创 2024-10-31 10:29
结果表明,这种肠道细菌酶可以减少肠道OEA——一种抑制食欲的化合物,这对营养不良儿童来说是非常有利的。
 如果有一种神奇的食物能够滋养肠道中的有益微生物,帮助营养不良的儿童更好地成长,那该有多好?这不,来自圣路易斯华盛顿大学医学院的研究人员就开发出了一种治疗性食物,这种食物可以改善儿童的生长和其他健康指标。为了弄清楚这种食物是如何起作用的,由医生科学家Jeffrey I. Gordon领导的一个研究小组深入研究了儿童肠道微生物组对这种疗法的反应。
如果有一种神奇的食物能够滋养肠道中的有益微生物,帮助营养不良的儿童更好地成长,那该有多好?这不,来自圣路易斯华盛顿大学医学院的研究人员就开发出了一种治疗性食物,这种食物可以改善儿童的生长和其他健康指标。为了弄清楚这种食物是如何起作用的,由医生科学家Jeffrey I. Gordon领导的一个研究小组深入研究了儿童肠道微生物组对这种疗法的反应。
相关研究结果发表在2024年10月25日的Science期刊上,论文标题为“A human gut Faecalibacterium prausnitzii fatty acid amide hydrolase”。
在这项新的研究中,Gordon团队发现了一种特殊的肠道细菌,它与孟加拉国儿童在接受一种旨在滋养健康肠道微生物的治疗性食物后更好地成长有关。这种以微生物为导向的治疗性食物被称为MDCF-2。研究人员发现,儿童肠道微生物群落中携带的这种细菌菌株拥有一种以前未知的基因,能够产生和代谢许多关键分子,这些分子参与调节食欲、免疫反应、神经元功能以及病原菌的致病能力。
Gordon说:“当我们通过修复儿童肠道微生物组来治疗营养不良时,我们有机会深入了解我们的微生物伙伴的内部运作。我们正在揭示肠道微生物如何影响我们身体的不同方面。这项研究表明,肠道微生物是生化大师,它们拥有我们一直没有意识到的代谢能力。”
更好地了解肠道微生物对人体的影响,可能为维护人类健康带来新的策略,并有助于指导针对多种疾病的治疗方法的开发。在两项随机对照临床试验中,研究人员发现了一系列微生物,它们的丰度和功能表达与参与者的生长改善相关。其中一种有益微生物是一种名为普氏栖粪杆菌(Faecalibacterium prausnitzii)的细菌。
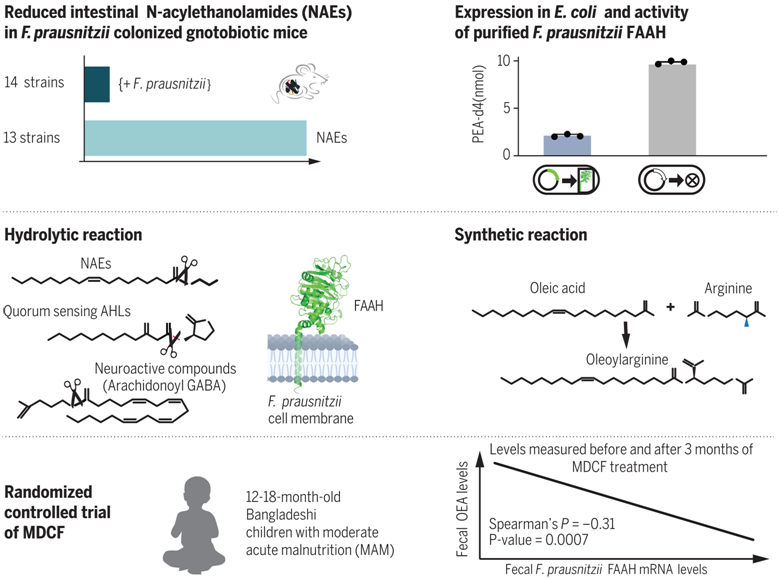
调控肠道内N-乙酰乙醇胺的普氏栖粪杆菌酶FAAH的发现和表征
论文共同第一作者Jiye Cheng博士和Sid Venkatesh博士对无菌条件下出生的小鼠进行了研究,然后将从孟加拉国儿童肠道微生物组中培养出来的微生物群落定植到这些小鼠体内。他们发现,在定植了特定普氏栖粪杆菌菌株的小鼠肠道中,油酰乙醇胺(Oleoylethanolamide, OEA)和十六酰胺乙醇(Palmitoylethanolamide, PEA)这两种分子的含量远远低于缺乏这种菌株的小鼠。值得注意的是,OEA和PEA是天然存在的脂质信号分子,已知在调节炎症、代谢和食欲方面发挥重要作用。
Gordon研究团队采用了一系列生物信息学和生物化学工具,确定了该细菌菌株产生的负责降解OEA和PEA的酶——脂肪酸酰胺水解酶(Fatty Acid Amide Hydrolase, FAAH)。人类版本的FAAH因其能够分解特定类型的神经递质——内大麻素(Endocannabinoids)而广为人知,并以此调节全身的人体生理机能。事实上,人类版本的FAAH是许多实验性药物的靶标,因为它在慢性疼痛、焦虑和情绪等神经状态中发挥作用。
Cheng和Venkatesh指出,普氏栖粪杆菌FAAH酶的发现代表了此类微生物酶的首个实例,并揭示了微生物在调节肠道中包括OEA和PEA在内的N-乙酰乙醇胺类重要分子水平中的作用。对在利用这种治疗性食物进行的临床试验中收集的营养不良儿童的粪便样本进行分析后发现,这种食物治疗导致OEA水平下降,同时增加了普氏栖粪杆菌的数量及其酶的表达。这些结果表明,这种肠道细菌酶可以减少肠道OEA——一种抑制食欲的化合物,这对营养不良儿童来说是非常有利的。
除了对这种治疗性食物的有益作用提供新的见解外,这篇论文还描述了这种细菌酶如何比人类FAAH具有更广泛的能力。这些能力包括合成脂质修饰氨基酸的独特能力,其中包括该团队展示的一些新分子,这些分子可以作为人类受体的调节剂,参与感知细胞的外部环境,以及作为肠道免疫反应的调节剂。此外,这种细菌酶还能控制其他含脂信号分子的水平,包括参与神经元间通讯的神经递质,以及致病细菌用来协调感染和破坏宿主免疫反应的所谓群体感应分子。
Gordon说:“人类FAAH和细菌FAAH的结构非常不同;有研究发现抑制人类FAAH的药物不会影响细菌FAAH。这为开发选择性操纵这种细菌酶的活性及其产物的新疗法打开了大门。这是微生物如何进化出我们人类基因组中没有编码但对人体正常功能仍很重要的功能的一个例子。我们现在知道,我们在两个不同的位置——人体细胞和肠道微生物组,拥有这种酶的两种不同版本。”
Gordon和他的同事、病理学与免疫学教授Michael Barratt博士强调,这种肠道细菌酶的鉴定为研究这种治疗性食物的有益效果提供了新的机会。Barratt还指出,除了处理正常饮食中的成分外,肠道中的这种酶还可能有助于解释不同个体对某些口服药物的反应差异。
Gordon总结道:“这种酶的微生物版本的作用之大令人惊讶。在未来的研究中,我们有兴趣探究这种酶在其他细菌基因组中的同源物是否可以补充FAAH或执行完全不同的活动。这些生物是化学大师,我们才刚刚开始探索它们能做什么。”
总之,这项研究不仅展示了肠道微生物在促进儿童健康成长方面的巨大潜力,还为未来的医疗创新提供了新的方向。随着更多研究的推进,我们有望看到更多营养不良及其他疾病得到有效的治疗,为患者带来更健康、更美好的生活。
(生物谷Bioon.com)
参考资料:
Jiye Cheng et al. A human gut Faecalibacterium prausnitzii fatty acid amide hydrolase. Science, 2024, doi:10.1126/science.ado6828.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


